
Ilaçi më i shitur i kompanisë Merck për astmën, Singulair, ka qenë i lidhur prej vitesh me vetëvrasje dhe probleme psikiatrike, shpesh tek fëmijët. Por paditë mbi ilaçin pengohen nga një nga mburojat më efektive të përgjegjësisë së Corporate America: doktrina e parandalimit federal.
Nga Dan Levine, Robin Respaut, Kristina Cooke, Mike Spector dhe Benjamin Lesser
Nicholas England, një 22-vjeçar i shëndetshëm nga Virxhinia, qëlloi veten në kokë në vitin 2017, më pak se dy javë pasi ai filloi të merrte një ilaç alergjie që ishte lidhur për vite me episode të depresionit dhe mendimit vetëvrasës.
Prindërit e tij së shpejti filluan të eksplorojnë një padi kundër Merck, zhvilluesit të ilaçit të suksesshëm të astmës dhe alergjive, Singulair, së bashku me prodhuesin e llojit gjenerik që mori djali i tyre. Nicholas nuk kishte histori të problemeve të shëndetit mendor, thanë ata.
England-ët u tronditën kur mësuan nga këshilltarët ligjorë se nuk mund të ngrinin asnjë padi. Ashtu si paditës të tjerë të panumërt të mundshëm, ata kishin hasur në një nga mburojat më efektive të përgjegjësisë së Corporate America: doktrinën ligjore të parandalimit, parimin sipas të cilit ligji federal zëvendëson ligjin shtetëror.

Nicholas England qëlloi veten për vdekje pasi mori një version gjenerik të Singulair për alergji sezonale. Rregullatorët amerikanë kanë marrë më shumë se 80 raporte për vetëvrasje të lidhura me ilaçin
Të armatosur me vendimet e Gjykatës së Lartë të SHBA-së për parandalimin duke filluar nga vitet 1990, kompanitë gjithnjë e më shumë argumentojnë se produktet ose shërbimet e rregulluara federale duhet të jenë të imunizuara nga paditë që pretendojnë shkelje të ligjit shtetëror.
Në një lexim të ri të një parimi të vjetër kushtetues, gjyqtarët kanë deklaruar se ligji federal, duke përfshirë vendimet e agjencive rregullatore të SHBA-së, duhet të parandalojë, ose të anashkalojë, statutet shtetërore që kërkojnë t’i mbajnë kompanitë përgjegjëse për dëmtimin e konsumatorëve.
Ligjet e shtetit, historikisht kanë ofruar bazën ligjore për disa nga paditë më të zakonshme kundër kompanive amerikane që pretendojnë lëndime, vdekje ose sëmundje të shkaktuara nga pakujdesia ose produkte me defekt.
Emocioni i humbjes së fëmijës është kaq i vështirë më vete. Është shumë zhgënjyese të kuptosh se është një zbrazëti. Unë jam një person i vogël në Virxhinia jugperëndimore dhe kjo është një zbrazëtirë atje për të mbrojtur kompanitë shumë më të mëdha se sa mund të luftonim.
Këto dinamika ligjore e lanë familjen England pa asnjë mjet juridik. Disa vendime të Gjykatës së Lartë të SHBA-së, në 2011 dhe 2013, në thelb ndaluan paditë kundër prodhuesve të barnave gjenerike bazuar në ligjet shtetërore që mundësonin pretendimet për defekte të dizajnit ose dështimin për të paralajmëruar konsumatorët për rreziqet e mundshme.
Arsyetimi i gjykatës: Pretendime të tilla u parandaluan nga rregulloret federale që parandalojnë prodhuesit e barnave gjenerike, kur kopjojnë barna të markave të emrit, të ndryshojnë formulimin ose etiketën paralajmëruese.
Kjo do të thoshte se Merck kishte shkruar etiketën paralajmëruese, me miratimin federal, në versionin gjenerik të Singulair që mori Nicholas England. Por prindërit e tij nuk mund të padisnin as Merck, sepse djali i tyre nuk e kishte marrë kurrë versionin e markës së saj të Singulair.
“Barra e humbjes së fëmijës tuaj është kaq e rëndë,” tha Jennifer England, nëna e Nicholas.
“Është shumë frustruese të kuptosh se është një zbrazëti. Unë jam një person pa peshë në Virxhinian jugperëndimore dhe ka një shteg atje për të mbrojtur kompanitë, shumë më i madh nga sa mund të luftojmë ne.
Merck nuk pranoi të komentonte për këtë raport, duke ia referuar të gjitha pyetjet Organon, një spinoff i Merck i krijuar në vitin 2021 që tani tregton Singulair. Organon kundërshtoi t’u përgjigjej pyetjeve të hollësishme nga Reuters, por tha në një deklaratë se ishte i bindur se mjekët dhe pacientët kanë marrë ‘informacion të plotë dhe të përshtatshëm’ mbi sigurinë e Singulair. Prodhuesi gjenerik i barnave që prodhoi pilulat që merrte England, Teva Pharmaceuticals, nuk iu përgjigj pyetjeve.
Mbrojtjet e parandalimit të korporatave kanë rezultuar gjerësisht efektive, sipas një analize të Reuters të rasteve gjyqësore dhe dhjetëra intervistave me avokatë, studiues ligjorë dhe paditës ose paditës të mundshëm të prekur nga vendimet e parandalimit.
Analiza e apelimeve federale dhe vendimeve të Gjykatës së Lartë që përfshinin parandalimin zbuloi se gjyqtarët vendosnin në dy të tretat e kohës për të dobësuar ose vrarë paditë që pretendonin vdekje ose lëndime të shkaktuara nga pakujdesitë e korporatave ose prodhime me defekt.
Mbrojtjet e parandalimit shpesh u japin kompanive një fitore të shpejtë procedurale, duke i lejuar ato të shmangin adresimin e thelbit të pretendimeve të paditësve. Është përdorur në një sërë sektorësh të rregulluar federalisht, nga hekurudhat tek kimikatet bujqësore tek linjat ajrore dhe automobilat, zbuloi rishikimi i Reuters.
Mbrojtja paraprake ka pasur një ndikim veçanërisht të thellë në industrinë farmaceutike, tregoi rishikimi. Ndalimi i gjykatës së lartë për disa padi kundër prodhuesve të barnave gjenerike ka shtrirje të jashtëzakonshme, sepse gjenerikët përbëjnë 91% të recetave në SHBA, sipas të dhënave nga Administrata e Ushqimit dhe Barnave të SHBA (FDA).
Prodhuesit e markave të barnave ende mund të paditen, por mbrojtja e parandalimit mund ta bëjë shumë më të vështirë për paditësit të triumfojnë, thanë ekspertët e çështjeve gjyqësore të industrisë farmaceutike. Në shumë raste të përgjegjësisë ndaj produktit, paditësit duhet të provojnë thjesht se produkti i një kompanie ishte i pasigurt.
Ata që përballen me mbrojtjen parandaluese të prodhuesve të barnave shpesh duhet të demonstrojnë se një kompani nuk arriti të zbulojë informacionin e sigurisë tek rregullatorët federalë – dhe se informacioni mund të ketë nxitur kufizime ose paralajmërime të reja qeveritare përpara se të ndodhte dëmi i supozuar.
Paditë në pritje kundër Merck pretendojnë se hulumtimi i hershëm i kompanisë tregoi se ilaçi mund të ndikojë në tru, por Merck minimizoi çdo rrezik në deklaratat për rregullatorët.
Familja England kishte shpresuar të detyronte drejtuesit nga Merck dhe prodhuesi gjenerik të tregonin atë që dinin dhe kur e dinin, mbi rreziqet e ilaçit. Në dekadën para vdekjes së England, FDA mori më shumë se 4,800 raporte të pacientëve, duke përfshirë shumë fëmijë, që përjetuan depresion, mendime vetëvrasëse ose probleme të tjera psikiatrike pas marrjes së Singulair ose një versioni gjenerik, sipas një rishikimi të të dhënave të FDA nga Reuters.
Por vetëm në vitin 2020, FDA-ja dha paralajmërimin e saj më serioz, të quajtur ‘kuti e zezë’, në etiketën e ilaçit. Në atë kohë, FDA kishte marrë më shumë se 80 raporte për vetëvrasje te njerëzit që merrnin ilaçin.
Singulair, një nga barnat më të shitura në historinë e SHBA, i ka siguruar Merck-ut rreth 50 miliardë dollarë të ardhura, tregojnë zbulimet e kompanisë. Që nga skadimi i patentës së Merck për Singulair në vitin 2012, prodhuesit kryesorë të barnave gjenerike kanë shitur miliona receta nën emrin shkencor të ilaçit, Montelukast.
FDA tha në një deklaratë se ka ‘mbikëqyrur me zell raportet e efekteve anësore që mund të lidhen me Montelukast, si dhe ka komunikuar gjetjet dhe ka ndërmarrë veprime rregullatore, kur është e përshtatshme’. Agjencia tha se ‘vazhdon të mbikëqyrë dhe hetojë këtë çështje të rëndësishme’.
FDA nuk pranoi të komentojë se si mbrojtja moderne e parandalimit dhe vendimet gjyqësore kanë ndikuar në rregullimin farmaceutik dhe proceset gjyqësore.

Këto janë pilulat kundër alergjive të marra nga Nicholas England, një 22-vjeçar, i cili qëlloi veten në vitin 2017, pak pasi nisi mjekimin. Prindërit e tij thonë se ai mori 12 doza, një në ditë, para se të vdiste nga vetëvrasja
Precedenti i madh në rastin e duhanit
Doktrina e parandalimit bazohet në klauzolën e supremacisë të Kushtetutës së SHBA. Synimi origjinal: të zgjidhë konfliktet midis statuteve federale dhe shtetërore dhe të dekurajojë legjislaturat e shtetit nga miratimi i ligjeve që minojnë politikën federale.
Mbrojtjet e korporatave të bazuara në parandalim janë një fenomen modern. Gjykatat amerikane i kanë parë historikisht paditë për përgjegjësinë e produktit, kryesisht të bazuara në ligjet e shtetit, si jetike për t’i mbajtur kompanitë përgjegjëse kur ligjet dhe rregulloret federale dështojnë ta bëjnë këtë.
Gjykatat njohën përgjegjësinë e prodhuesve të barnave për ilaçet e dëmshme që në vitet 1850, sipas një dosjeje të Gjykatës së Lartë. Rregulloret e FDA-së dikur specifikonin në mënyrë rutinore se vendimet e saj nuk kishin ndikim në përgjegjësinë e prodhuesve të barnave.
Kjo filloi të ndryshojë në vitin 1992, në një rast që përfshinte një duhanpirës që vdiq nga kanceri. Gjykata e Lartë vendosi që kërkesat federale për etiketat e cigareve, të cilat kishin përfshirë paralajmërimet për pirjen e duhanit që nga vitet 1960, shkelnin disa nga pretendimet e ligjit shtetëror të familjes se një kompani duhani nuk e paralajmëroi atë për rreziqet e pirjes së duhanit.
Shtetet në fund përdorën teori të ndryshme për të detyruar Big Tobaço në një marrëveshje prej 246 miliardë dollarësh. Prapëseprapë, precedenti i dha ‘Corporate America’ një plan për të mposhtur padi të ngjashme për arsye parandalimi.
Korporatat morën më shumë ndihmë në arenën politike. Presidenti i SHBA-së Xhorxh W. Bush kishte premtuar në fushatën e tij të vitit 2000 se do sulmonte atë që republikanët e përqeshnin si një proces gjyqësor joserioz që synonte të godiste industrinë amerikane.
Zyrtarët e administratës ndërmorën atë që kritikët e quajtën reformën e delikteve ‘të fshehta’: ndërhyrja në padi nga ana e të pandehurve të korporatave, me qëllimin për të bindur gjyqtarët për të vendosur precedentë duke e bërë më të vështirë padinë ndaj kompanive.
FDA e Bushit ilustron taktikën. Daniel Troy, këshilltari kryesor i agjencisë, e interpretoi parandalimin që do të thotë se gjykatat nuk mund të minojnë rregullatorët federalë bazuar në shkeljet e supozuara të ligjit shtetëror.
Ai synonte ta bënte këtë argument në procese gjyqësore të profilit të lartë. Në një konferencë të vitit 2003, Troy ftoi një audiencë avokatësh të industrisë së barnave për të lëkundur FDA-në për të ndërhyrë në rastet e tyre.
“Ne nuk mund të përballojmë të përfshihemi në çdo rast – ne duhet të zgjedhim ku duhet përdorur ‘fishekët’,” u tha ai avokatëve të mbledhur.
“Pra, bëjeni të tingëllojë si një ngrehinë Hollivudi.”
Troy, tani një avokat veteran i industrisë farmaceutike, tha se qëllimi i tij në atë kohë ishte thjesht të mbronte dhe forconte autoritetin e FDA-së për të rregulluar pa ndërhyrje.
“Nëse besoni në një FDA të fortë,” tha ai, “ne nuk mund të kemi gjykatat shtetërore, veçanërisht juritë, që hamendësojnë dhe nënvlerësojnë gjykimet e FDA”.
FDA ndryshoi zyrtarisht pikëpamjen e saj për parandalimin në një rregullore të vitit 2006, duke deklaruar se agjencia tani besonte se miratimi i etiketimit të FDA ‘parandalon ligjin kundërshtues ose të kundërt të shtetit’.
Në deklaratën e saj për Reuters, FDA nuk pranoi të komentojë rregulloren e vitit 2006 ose pikëpamjen e tanishme të agjencisë për parandalimin.
Një nga fitoret më të mëdha të FDA-së të epokës së Bushit erdhi në vitin 2008, kur Gjykata e Lartë përmendi parandalimin në rrëzimin e padisë së një burri në Nju Jork kundër Medtronic për një kateter të balonës. Precedenti që atëherë ka ndaluar në mënyrë efektive një pjesë të gjerë të padive kundër prodhuesve të pajisjeve mjekësore.

Pacientët dhe prindërit e pacientëve që morën ilaçin e Merck, Singulair thonë se kompania dhe FDA nuk arritën të vepronin për vite me radhë në përgjigje të raporteve për vetëvrasje dhe probleme psikiatrike të lidhura me ilaçin e astmës dhe alergjisë
Për të shqyrtuar ndikimin e mbrojtjeve paraprake, Reuters shqyrtoi 257 ankesa federale dhe vendime të Gjykatës së Lartë, të cilat janë më me ndikim në krijimin e precedentëve. Në rastet, që datojnë që nga viti 2001, gjykatat përcaktuan nëse parapagimi anuloi pretendimet e paditësve se vdekjet ose dëmtimet ishin shkaktuar nga pakujdesia e korporatës ose produkte me defekt. Gjyqtarët hodhën poshtë disa ose të gjitha pretendimet mbi bazën e parablerjes në dy të tretat e rasteve.
Një përfitim tjetër i industrisë nuk mund të llogaritet sasior: Numri i padive të mundshme që nuk u ngritën kurrë – si ajo për vdekjen e Nicholas England – sepse precedentët e parandalimit favorizojnë korporatat, thanë ekspertët ligjorë.
Adam Zimmerman, një profesor në Shkollën e Drejtësisë Gould të Universitetit të Kalifornisë Jugore, tha se analiza e Reuters nënvizon se si këta precedentë të parandalimit, të cilët lidhin gjykatat më të ulëta, u kanë dhënë korporatave fitore të rëndësishme në sallën e gjyqit dhe leva në negociatat e zgjidhjes së çështjeve.
“Është vërtet domethënëse për komunitetin e biznesit,” tha Zimmerman.
Jay Lefkoëitz, një partner i Kirkland & Ellis, i cili ka përfaqësuar kompanitë përpara Gjykatës së Lartë, e quajti parandalimin një parim kushtetues ‘të sanksionuar fort’. Juritë e gjykatës shtetërore, tha ai, nuk duhet të vendosin se si lexohen etiketat e ilaçeve bazuar në provat në një rast.
“Ne duam që shkencëtarët dhe mjekët në FDA ta bëjnë këtë,” tha ai, “bazuar në të gjitha të dhënat e grumbulluara nga provat klinike dhe përvojën e botës reale.”
Rrënojat e trenit
Mbrojtjet e parandalimit të korporatave tani janë të zakonshme në një mori industrish të rregulluara në mënyrë federale.
Pas daljes nga shinat e një treni në shkurt në Palestinën Lindore, Ohio, duke lëshuar kimikate toksike, operatori i trenit, Norfolk Southern kërkoi parandalimin për t’iu kundërvënë padive në pritje.
E pyetur për strategjinë ligjore, kompania i tha Reuters se ‘po ndiqte procesin ligjor’ dhe se ishte e angazhuar të paguante për pastrimin e mjedisit dhe çdo dëmtim të shëndetit të banorëve, furnizimit me ujë ose vlerave të pronës.

Ky filmim nga një video e qeverisë tregon daljen nga shinat e trenit në shkurt në Palestinën Lindore, Ohio, i cili lëshoi kimikate toksike. Operatori i trenave Norfolk Southern ka përdorur doktrinën ligjore të parandalimit për t’u mbrojtur nga paditë për incidentin
Analiza e Reuters gjeti rreth tre duzina shembuj gjatë dy dekadave të fundit të kompanive në industrinë e hekurudhave që thirren paraprakisht për të shmangur përgjegjësinë. Ata citojnë ligjet federale që rregullojnë sigurinë e hekurudhave dhe transportit të materialeve të rrezikshme.
Në vitin 2015, për shembull, një tren i Union Pacific goditi një kamionçinë në Luiziana, duke vrarë tre persona, sipas të dhënave të gjykatës. Shoferi i kamionit ishte i fundit në një kolonë, duke pritur të kalonte përmes një porte që ende nuk ishte hapur. Disa sekonda më vonë, një tren i Union Pacific doli nga shinat me rreth 50 milje në orë.
Familjet e viktimave të aksidentit paditën dhe humbën, pjesërisht për shkak se Akti Federal i Sigurisë Hekurudhore parandaloi pretendimet e tyre se boria e shtypur nga konduktori nuk arriti të paralajmëronte siç duhet ardhjen e trenit.
Paditësit kishin argumentuar se rënia më e shpeshtë e borisë, për shembull, do kishte qenë më efektive. Një gjykatë apeli vendosi se çështja e tyre ishte e parandaluar sepse rregullorja federale e shtyn ‘gjykimin e vetëm’ të një inxhinieri për t’i rënë borisë në raste të tilla.
Union Pacific tha në një deklaratë se inxhinieri ishte në përputhje me ligjin federal dhe se parandalimi siguron një ‘ligj të qëndrueshëm dhe uniform’ për operatorët e trenave që transportojnë mallra nëpër linjat shtetërore.
Në një rast tjetër farmaceutik që përfshin vetëvrasjen, një grua, burri i së cilës u hodh para një treni pak pasi ai filloi të merrte antidepresantin paroxetine, u ndalua nga parandalimi që të padiste prodhuesin gjenerik.
Më pas, një gjykatë apeli përmendi parandalimin për të përmbysur një vendim prej 3 milionë dollarësh që gruaja kishte fituar kundër GlaxoSmithKline, e cila bëri versionin e markës së drogës dhe kontrollonte etiketën e saj. Gjykata zbuloi se FDA do të kishte refuzuar një paralajmërim për vetëvrasje të të rriturve në kohën kur burri i saj e mori ilaçin.
GlaxoSmithKline tha në një deklaratë se parandalimi është një ‘parim ligjor i vendosur mirë i bazuar në Kushtetutën e SHBA-së’ për të adresuar konfliktet midis ligjit federal dhe atij shtetëror. Kompania tha se i kërkoi vazhdimisht FDA-së të shtonte një paralajmërim për mendimin vetëvrasës tek të rriturit në etiketë, por agjencia refuzoi. FDA në vend të kësaj mandatoi të njëjtën etiketë për të gjitha barnat që përfshinin paroxetine, e cila nuk përfshinte një paralajmërim të tillë.
Gjiganti bujqësor Monsanto tani po i mbështet shpresat e tij te parandalimi për të ndihmuar në mposhtjen ose dobësimin e dhjetëra mijëra pretendimeve ligjore që pretendojnë se nuk i paralajmëroi konsumatorët se vrasësi i tij popullor i barërave të këqija Roundup mund të shkaktojë kancer.
Në qershor, kompania, në pronësi të Bayer, i kërkoi gjykatës federale të apelit në Atlanta të pushonte një nga ato raste për arsye parandalimi, duke argumentuar se rregullatorët federalë nuk kërkonin një paralajmërim për kancerin në etiketën e Roundup.
Bayer tha në një deklaratë se këto pretendime të bazuara në shtet janë të parandaluara sepse ligji federal i ndalon shprehimisht shtetet të vendosin kërkesa të ndryshme etiketimi. Rregullatorët federalë, tha Bayer, kanë gjetur vazhdimisht se Roundup dhe herbicidet e ngjashme mund të përdoren në mënyrë të sigurtë dhe nuk janë kancerogjene.
Ndërsa precedentët e parandalimit favorizojnë korporatat, toleranca e gjyqtarëve për argumentin ka kufijtë e saj. Gjykata e Lartë në vitin 2009 hodhi poshtë pretendimin nga prodhuesi i drogës Ëyeth, së bashku me grupet e industrisë, se miratimi i FDA duhet t’u japë prodhuesve të markave të emrit imunitet të plotë nga disa lloje të padive. Gjykata vendosi në favor të një gruaje nga Vermonti e cila pretendoi se ilaçi i firmës Phenegran çoi në amputimin e krahut të saj.
‘Unë po e helmoja’
Mbrojtja e parandalimit mbështetet pjesërisht në nocionin se ligjet shtetërore nuk janë të nevojshme për të mbrojtur qytetarët që tashmë mbrohen nga rregullatorët federalë. Por në rastin e efekteve anësore potencialisht vdekjeprurëse të Singulair, FDA priti vite, pavarësisht mijëra problemeve psikiatrike të raportuara, për të kërkuar paralajmërimin e saj më serioz në etiketën e ilaçit.
Në kohën kur Nicholas England vrau veten, FDA kishte rishikuar zbulimet e Merck në lidhje me rreziqet shëndetësore për gati dy dekada. Prindërit që argumentojnë se Singulair rrezikoi fëmijët e tyre, e shohin vendimin e FDA-së për vitin 2020 për të shtuar një paralajmërim ‘të kutisë së zezë’ si justifikim, por shumë ende dëshirojnë të padisë Merck-un që nuk veproi më shpejt.
Në vitet pas fillimit të Singulair në 1998, raportet e episodeve neuropsikiatrike të lidhura me të u grumbulluan në forumet e internetit dhe në sistemin e zbulimit të paralajmërimit të hershëm të FDA-së. Sistemi përpilon raporte të ‘efekteve të padëshiruara’ nga pacientët, mjekët dhe të tjerët për të gjurmuar rreziqet e mundshme të zbuluara pasi një ilaç del në treg.
Djalit të Jan Gilpin iu dha për herë të parë Singulair për astmë në vitin 2003, në moshën tre vjeçare. Djali shpejt u duk i tërhequr dhe i mërzitur. Ai ndonjëherë kalonte ‘në një ekstazë të çuditshme, duke mërmëritur me veten’, shkroi Gilpin në 2008 në një raport për FDA.
“Më e keqja nga të gjitha, ai filloi të fliste për vdekjen, duke dashur të vdiste, duke dashur të kishte vdekur, duke thënë se e urrente veten.”
“E kuptova se ai nuk kishte qeshur për dy vjet. Nuk e kuptova që po e helmoja me këtë ilaç.”
Gilpin nuk dyshoi për Singulair për më shumë se tre vjet. Në vitin 2007, ajo ndaloi t’i jepte djalit të saj ilaçin pasi gjeti postimet e prindërve në internet në lidhje me fëmijët e tyre që përjetonin ankth social ndërsa merrnin ilaçin.
Së shpejti, ajo vuri re se ai filloi të kapërcejë gjendjen dhe të qeshë.
“E kuptova se ai nuk kishte qeshur për dy vjet,” tha Gilpin, duke folur mes lotësh.
“Nuk e kuptova që po e helmoja me këtë ilaç.”
Mendimet obsesive të djalit për vdekjen u zhdukën pasi ai e la ilaçin, tha Gilpin, por ai dukej se kishte disa efekte të vazhdueshme, të tilla si ankthi, që iu desh më shumë për t’u larguar.

Jan Gilpin tregon fotografitë e djalit të saj, ndërkohë që ai po merrte ilaçin Singulair për të trajtuar astmën
Në gusht të vitit 2007, një djalë 15-vjeçar në Nju Jork vrau veten 17 ditë pasi mori për herë të parë Singulair. Dy muaj më vonë, Merck propozoi dhe FDA ra dakord, të ndryshonte etiketën e Singulair duke shtuar mendimin dhe sjelljen vetëvrasëse në listën e efekteve negative të raportuara.
Por përmendja e të menduarit vetëvrasës u shfaq në mes të një liste me më shumë se tre duzina efekte anësore. Mbrojtësit e prindërve argumentojnë se etiketa e re ishte jashtëzakonisht e pamjaftueshme për të paralajmëruar për një rrezik kaq të madh.
Tre javë pasi propozoi ndryshimin e etiketës, Merck i kërkoi FDA-së për marrjen e lejes për të shitur Singulair pa recetë, pa recetë, për të rriturit me alergji nga poleni. FDA ra dakord ta konsideronte atë, por gjithashtu donte të kuptonte më shumë rreth rreziqeve të vetëvrasjes.
Një rishikim i FDA i vitit 2008 i ndikimeve psikiatrike të drogës dhe rreziqeve të vetëvrasjes rekomandoi “studime të mëtejshme te kafshët dhe njerëzit” dhe sugjeroi që agjencia të konsideronte t’i kërkonte Merck-ut të kryente një studim vëzhgues.
FDA nuk kërkoi një studim të tillë, duke arsyetuar pjesërisht se efektet anësore serioze, duke përfshirë mendimin vetëvrasës ‘pritej të ishin mjaft të rralla’.
Në vitin 2011, agjencia hodhi poshtë një peticion nga Gilpin dhe prindër të tjerë që kërkonin një paralajmërim ‘të kutisë së zezë’, duke përmendur atë që e quajti prova të pamjaftueshme që ilaçi shkaktonte sjellje vetëvrasëse.
82 vetëvrasje
Pasi patenta e Merck për Singulair skadoi në vitin 2012, prodhuesit gjenerikë filluan të prodhonin ilaçin. Sipas FDA, numri i pacientëve të cilëve u është dhënë ilaçi u rrit nga rreth 7 milionë në vit në më shumë se 9 milionë. Disa vite, gati gjysma e këtyre pacientëve ishin 16 vjeç ose më të rinj.
FDA mblodhi një panel këshillues në 2014 për të shqyrtuar kërkesën e Merck për të ofruar Singulair pa recetë. Me kërkesë të FDA-së, Merck kishte rianalizuar të dhënat e provës klinike të Singulair në vitin 2009.
Kompania kishte raportuar se një pjesëmarrëse e proves, 18-vjeçare kishte tentuar vetëvrasjen dhe një 12-vjeçare ishte shtruar në spital për depresion dhe mendime vetëvrasëse. Në të dyja rastet, hetuesi gjykues përcaktoi se ngjarjet nuk kishin lidhje me Singulair. Në vitin 2014, Stephane Bissonnette, një menaxher i Merck-ut në atë kohë, i tha panelit të FDA se ‘vetëvrasja ishte mjaft e rrallë’ në prova.
FDA gjithashtu analizoi të dhënat e Merck dhe në përgjithësi ra dakord me përfundimin e saj, megjithëse agjencia pranoi se provat ishin të shkurtra dhe nuk ishin të modeluara për të zbuluar efektet neuropsikiatrike.
Paneli i FDA rekomandoi refuzimin e kërkesës për të shitur Singulair pa recetë për shkak të shqetësimeve të sigurisë. Paneli gjithashtu bëri thirrje për studime të reja mbi efektet anësore neuropsikiatrike, një regjistër pacientësh dhe një vlerësim se sa mirë pacientët e kuptonin etiketën e Singulair.
FDA numëroi 82 vetëvrasje të lidhura me Singulair dhe versionet e tij gjenerike të raportuara në bazën e të dhënave të saj të ngjarjeve të padëshiruara që nga viti 1998. Vetëm 64 prej raporteve jepnin një moshë; prej tyre, 31 përfshinin dikë 19 vjeç ose më të ri.
“Raportet e efekteve anësore neuropsikiatrike “me të vërtetë duhet të na bëjnë të ndalemi se mund të ketë diçka që ne nuk e kuptojmë,” tha Dr. Judith Kramer, profesoreshë mjekësore në Duke dhe një anëtare e komitetit këshillues, në takimin e 2014-ës.
FDA ndoqi vetëm gjysmën e rekomandimit: Ajo nuk pranoi të autorizonte shitjet pa recetë, por gjithashtu refuzoi të urdhëronte studime të reja, pjesërisht sepse efektet anësore neuropsikiatrike ishin tashmë një ‘çështje e njohur e sigurisë’, tha një zyrtar i sigurisë së agjencisë në atë kohë.
FDA i tha Reuters se refuzoi të urdhëronte më shumë kërkime për shkak të ‘shqetësimeve të fizibilitetit’.
Në vitin 2019, FDA mblodhi një tjetër panel këshillues nëse efektet anësore të ilaçit meritonin një paralajmërim ‘të kutisë së zezë’. Përpara takimit, FDA numëroi 82 vetëvrasje të lidhura me Singulair dhe versionet e tij gjenerike të raportuara në bazën e të dhënave të saj të ngjarjeve të padëshiruara që nga viti 1998. Vetëm 64 nga raportet jepnin një moshë; prej tyre, 31 përfshinin dikë 19 vjeç ose më të ri.
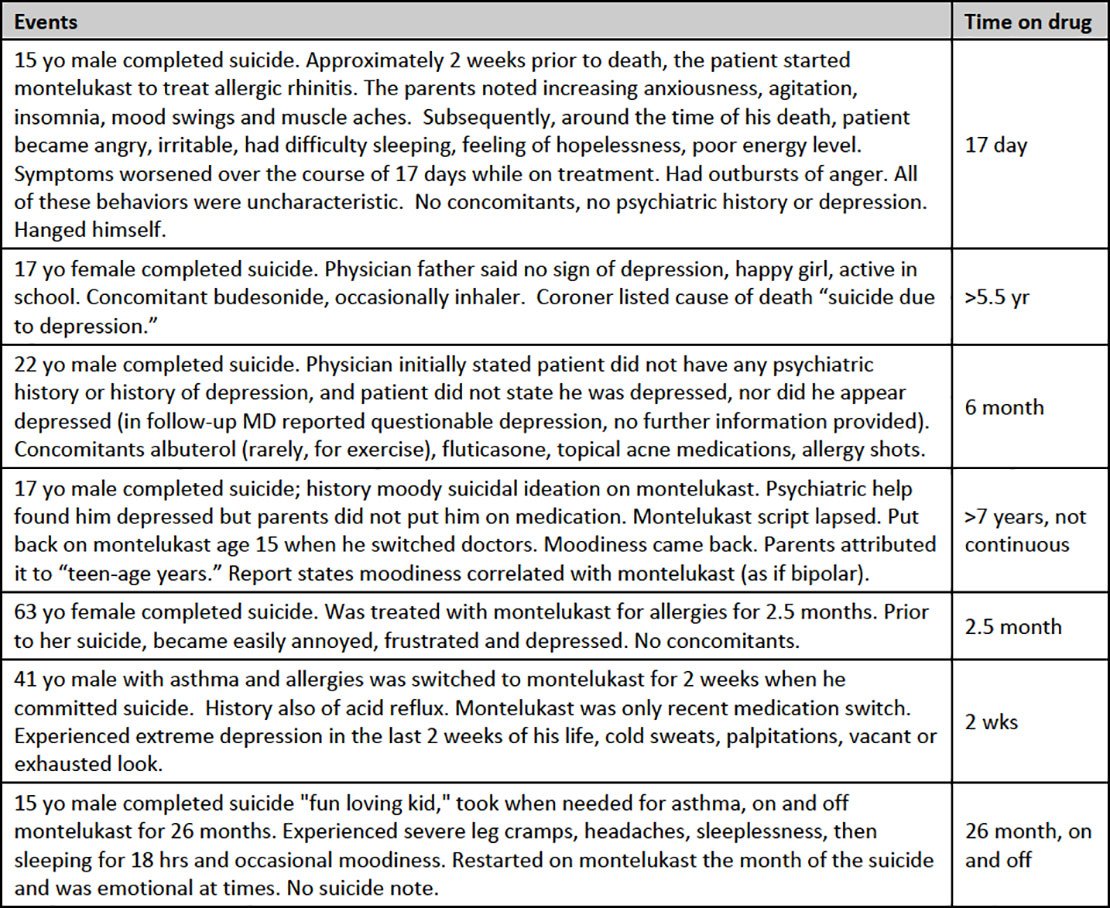
Tregime të përfshira në raportet e FDA-së për vetëvrasjet që lidhen me ilaçin e astmës dhe alergjisë së Merck, Singulair ose versione gjenerike. Agjencia regjistroi incidentet në bazën e të dhënave të saj të ‘efekteve të padëshiruara’, e cila gjurmon efektet anësore potencialisht problematike të ilaçit
Megjithatë, punonjësit e agjencisë përsëri thanë se nuk kishte prova të mjaftueshme për të merituar një paralajmërim ‘të kutisë së zezë’, duke vënë në dukje se etiketa tashmë paralajmëroi për efekte të mundshme neuropsikiatrike.
Stafi i FDA-së pranoi se agjencia kishte autoritetin të kërkonte studime të reja. Por Merck tani kishte pak nxitje për të kryer kërkime të shtrenjta, sepse patenta e saj për Singulair kishte skaduar dhe fitimet e saj nga ilaçi kishin rënë. Në vend të kësaj, Merck thjesht mund ta tërheqë Singulair nga tregu, i tha një zyrtar i FDA-së komitetit këshillues në 2019.
Në vend që të kërkonte studime të reja, FDA njoftoi në mars 2020 se do shtonte ‘një kuti të zezë’ në etiketat e Singulair dhe variacionet e tij gjenerike, duke paralajmëruar për efekte anësore serioze neuropsikiatrike, duke përfshirë mendimin dhe sjelljen vetëvrasëse. Agjencia citoi një hulumtim të pavarur nga viti 2015 që tregon shpërndarjen e drogës në tru. FDA këshilloi kufizimin e përdorimit të ilaçit për trajtimin e alergjive, duke thënë se nuk duhet të jetë trajtimi i parë.

Selia e Merck në Kenilworth, New Jersey. FDA në vitin 2020 kërkoi etiketën e saj më serioze – një “kuti e zezë” – për ilaçin më të shitur të Merck për astmën dhe alergjinë, Singulair, për shkak të shqetësimit për mendimin vetëvrasës dhe efektet e tjera anësore psikiatrike
‘Kjo nuk ka kuptim’
Reuters intervistoi 16 pacientë ose prindërit e tyre që dyshojnë se Singulair ka shkaktuar efekte anësore psikiatrike. Shumë, si Nicholas England, morën një version gjenerik. England u rrit në qytetin rural të Wise, Virxhinia.
Ai ishte i qetë dhe fizikisht i aftë dhe refuzonte ushqime të pashëndetshme kur pjesa tjetër e familjes po e hante atë, tha babai i tij, Robert England. Ai besonte se djali i tij mund të kishte vështirësi për të fjetur pas marrjes së ilaçit, por përndryshe dukej normal.
Pasi Nikolas vdiq, një raport i policisë vuri në dukje se ai nuk kishte drogëra të paligjshme në sistemin e tij. Rasti i hutoi hetuesit, tha Robert: “Të gjithë këta djem më shikuan dhe më thanë: Kjo nuk ka kuptim”.
Në vitet kur FDA vonoi veprimin për Singulair, disa prindër filluan të kontaktojnë avokatët për të eksploruar marrjen e masave ligjore. Shumica, si familja England, u ndaluan nga precedentët e gjykatës të padisnin sepse fëmijët e tyre morën një version gjenerik të drogës. Kim Beck, një avokate që përfundimisht ngriti qindra padi kundër Merck për Singulair, tha se firma e saj largoi mijëra klientë të tjerë potencialë që kishin marrë barna gjenerikë.
Veprimi rregullator i FDA-së i vitit 2020 inkurajoi disa pacientë të padisnin Merck. Shumica e këtyre padive janë në fazat e hershme, por Merck ka pasur njëfarë suksesi me mbrojtjen paraprake.
Në Wisconsin, për shembull, një nënë paditi Merck në vitin 2020 duke pretenduar se Singulair shkaktoi që djali i saj të institucionalizohej me depresion të rëndë. Djalit iu përshkrua Singulair në vitin 2010, por kaloi në versionin gjenerik në 2012.
Merck argumentoi se paditësi nuk mund të tregonte se FDA do kishte miratuar një paralajmërim më të fortë përpara vitit 2012, kur djali po merrte emrin e markës Singulair. Prodhuesi i drogës përmendi refuzimin e peticionit nga agjencia në vitin 2011 nga Gilpin dhe prindër të tjerë për të shtuar një paralajmërim të tillë.
Një gjykatës ra dakord, duke vendosur se ‘ligjet përkatëse federale dhe shtetërore në këtë rast bien ndesh në mënyrë të papajtueshme’. Ai hodhi poshtë pothuajse çdo kërkesë në padi, të cilën nëna më pas e hodhi poshtë.
Merck akuzohet se ka minimizuar provat e hershme të ndikimit në tru të ilaçit
Një reklamë e hershme e revistës për ilaçin e njohur Merck për astmën dhe alergjinë, Singulair, paraqiste një fëmijë të lumtur, të varur me kokë poshtë nga një pemë. Fëmijët astmatikë tani mund të merrnin frymë më lehtë, shkruante teksti, dhe efektet anësore ishin ‘zakonisht të lehta’ dhe ‘të ngjashme me një pilulë sheqeri’.
Kur ilaçi u hodh në treg në vitin 1998, etiketa e saj thoshte se shpërndarja e ilaçit në tru ishte ‘minimal’, pa përmendur efektet anësore psikiatrike.
Pretendimet e hershme të sigurisë të Merck u përballën më vonë me një shqyrtim intensiv mes raporteve mbi dy dekada se pacientët, përfshirë shumë fëmijë, kishin vdekur nga vetëvrasja ose kishin përjetuar probleme neuropsikiatrike pas marrjes së ilaçit. FDA në vitin 2020 urdhëroi paralajmërimin e saj më serioz, të njohur si ‘kuti e zezë’, në etiketën e Singulair.
Dhe Merck tani përballet me një sërë padish që pretendojnë se e dinte nga kërkimet e saj të hershme se ilaçi mund të ndikonte në tru dhe se minimizonte potencialin për probleme psikiatrike në deklaratat për rregullatorët.
Paditë citojnë kërkimin e Julia Marschallinger, një biologe qelizore e cila ka studiuar ilaçin së bashku me kolegët në Institutin e Mjekësisë Rigjeneruese Molekulare në Austri. Ai ekip zbuloi në vitin 2015 se shpërndarja e drogës në tru ishte më domethënëse sesa përshkruhej në etiketën e saj. FDA citoi punën e Marschallinger kur porositi etiketën paralajmëruese të ‘kutisë së zezë’ të Singulair.
Në patentën e saj origjinale për Singulair, Merck përmendi aplikime të tjera për ilaçin, përtej astmës dhe alergjive, duke përfshirë si një trajtim për ‘spazmën cerebrale’, një gjendje neurologjike. Paditë e ngritura kundër Merck citojnë këtë patentë të vitit 1996 si dëshmi e njohurive të Merck për ndikimet e mundshme të ilaçit në trur.
Merck nuk pranoi të komentojë për këtë raport.
Në vitin 2014, shkencëtarët në Austri rianalizuan studimet origjinale të Merck për kafshët dhe vunë re se ilaçi u ul pothuajse kudo në trup 24 orë pas dozës – por jo në tru, ku u rrit.
Kur Merck kërkoi për herë të parë miratimin e FDA-së për Singulair, një analist i FDA, duke u mbështetur në pohimet e kompanisë, tha në vitin 1998 se ‘vetëm një sasi gjurmë’ e ilaçit mund të gjendej në tru, tregojnë dokumentet federale. FDA tha se të dhënat e Merck treguan se prania e Singulair ‘ka rënë me kalimin e kohës’ në të gjitha indet.
Marschallinger dhe kolegët e saj në Austri dolën me një gjetje të ndryshme kur rishikuan kërkimin origjinal të Merck dhe bënë disa kërkime të tyret. Ata filluan ta shikonin Singulair si një trajtim të mundshëm të çmendurisë në vitin 2011.
Ata u interesuan për këtë perspektivë pjesërisht për shkak të raporteve të efekteve anësore psikiatrike, si depresioni, agjitacioni ose halucinacionet, nga pacientët dhe ofruesit mjekësorë. Ndërsa ishte shqetësuese, efektet anësore treguan se ilaçi mund të ndikojë në tru. Studiuesit donin të kuptonin nëse nga kjo mund të përfitonin pacientët e moshuar me demencë.
Në vitin 2014, shkencëtarët në Austri rianalizuan studimet origjinale të Merck për kafshët dhe vunë re se ilaçi u ul pothuajse kudo në trup 24 orë pas dozës – por jo në tru, ku u rrit gjatë kësaj periudhe, duke tejkaluar sasinë si në gjak ashtu edhe në mushkëri. Ajo raportoi se zbuloi se një ‘sasi e konsiderueshme’ e drogës kishte arritur në tru, në kontrast me përshkrimin e Merck për shpërndarjen në tru si ‘minimale’.
FDA tha se studimet origjinale të Merck për kafshët ishin ‘mjaft të kufizuara dhe nuk mund të japin ndonjë informacion përfundimtar në lidhje me nivelet dhe aktivitetin e montelukastit në tru’. Agjencia pranoi se përshkrimi i recensuesit të saj se nivelet e ilaçit ranë me kalimin e kohës në të gjitha indet ‘nuk pasqyronte plotësisht të dhënat’.
Sa i përket konstatimit të Marschallinger se një ‘sasi e konsiderueshme’ e ilaçit kishte arritur në tru, FDA e quajti atë ‘një karakterizim subjektiv që nuk është domosdoshmërisht i papajtueshëm me përshkruesin ‘minimal’ në kontekste të tjera’. Studimi i 2015 i shkëncëtarëve, tha FDA, siguroi prova shtesë se ilaçi arriti në tru, por nuk tregoi ndonjë dëm specifik.
Marschallinger tha se do kishte qenë logjike që FDA t’i kërkonte Merck-ut të hetonte ndikimet në tru në mënyrë më të hollësishme pasi të dilnin raporte për probleme të shëndetit mendor.
“FDA mund t’i kishte kërkuar Merck-ut të përsëriste eksperimentin ose ta bënte atë për një periudhë edhe më të gjatë kohore,” tha Marschallinger. “Nuk është e vështirë ta bësh këtë.”
Metodologjia
Reuters u përqendrua në apelimet federale dhe vendimet e Gjykatës së Lartë për të matur suksesin e mbrojtjes paraprake në paditë që pretendonin se pakujdesia e korporatës ose produktet me defekt shkaktuan lëndime ose vdekje. Këto raste janë të rëndësishme sepse ato zakonisht krijojnë precedentë ligjorë që gjyqtarët e tjerë në të gjithë Shtetet e Bashkuara duhet të ndjekin.
Gazetarët punuan me një specialist në Westlaw, një shërbim kërkimor ligjor në pronësi të Thomson Reuters, për të identifikuar rastet që nga viti 2001 që përfshinin mbrojtjen. Ata kërkuan bazën e të dhënave të Westlaw të vendimeve të gjykatave federale për opinione që përmbanin frazën ‘parandaloj’ si dhe fjalë ose fraza kyçe shtesë, të tilla si ‘përgjegjësi ndaj produktit’, ‘pakujdesi’, ‘përgjegjësi e rreptë’ dhe ‘dështim për të paralajmëruar’. Gazetarët u këshilluan me disa ekspertë ligjorë të jashtëm në zhvillimin e termave të kërkimit.
Kërkimet dhanë rreth 800 opinione që një ekip gazetarësh të Reuters i shqyrtoi manualisht për të përcaktuar nëse mbrojtja parandaluese ishte në diskutim në opinion dhe nëse rasti përfshinte pretendime për lëndim fizik të paktën një personi. Rishikimi e ngushtoi sasinë e mundshme në 257 raste përkatëse.
Gazetarët më pas lexuan çdo opinion në ato 257 vendime për të përcaktuar rezultatin e mbrojtjes paraprake. Ata i shënuan rastet ‘të suksesshme’ kur gjyqtarët pranuan të gjitha kërkesat për parandalim. Rastet u shënuan ‘pjesërisht të suksesshme’ kur disa pretendime ishin paraprakisht, por të tjerët jo. Rastet u shënuan si ‘të pasuksesshme’ kur asnjë pretendim nuk ishte paraparë.
Çdo opinion u shqyrtua veçmas nga dy raportues për të siguruar saktësinë e kodimit.
VINI RE: Ky material është pronësi intelektuale e Reuters
Përgatiti për Hashtag.al, K.Manjani



























