Majtas kreu i Pfizer Albert Bourla, djathtas kreu i BionTech Ugur Sahin
Pfizer dhe BioNTech ndaluan një studim të madh në Shtetet e Bashkuara për vaksinën e përditësuar kundër COVID-19 tek të rritur të shëndetshëm të moshës 50 deri 64 vjeç, duke deklaruar se regjistrimi i pjesëmarrësve ishte shumë i ulët për të prodhuar të dhënat e nevojshme.
Në një letër drejtuar hetuesve të studimit, të datës 30 mars dhe të parë nga Reuters, Pfizer tha se do të ndalonte monitorimin për shenja të sëmundjes COVID për të gjithë pjesëmarrësit pas 3 prillit.
Regjistrimi u mbyll më 6 mars, pas një rishikimi të tendencave aktuale epidemiologjike, thuhej në letër.
Ky vendim vjen në një kohë kur prodhuesit e vaksinave kundër COVID po përballen me rezistencë nga administrata amerikane dhe me kërkesë të dobët për vaksinat në SHBA.
FDA vitin e kaluar ashpërsoi kërkesat për përdorimin e vaksinave kundër COVID, duke kërkuar prova të mëdha klinike me placebo për grupmoshën 50–64 vjeç, në mënyrë që vaksina të përfshihej në rekomandime.
Pfizer dhe BioNTech i thanë Reuters se kishin informuar FDA-në për qëllimin e tyre për të ndalur studimin, duke përmendur vështirësitë për të gjetur mjaft pjesëmarrës. Synimi ishte të përfshiheshin rreth 25,000 deri 30,000 persona.
“Ky studim nuk po përfundon për shkak të ndonjë shqetësimi mbi sigurinë apo balancën përfitim-rrezik. Synojmë ta ndalim për shkak të ritmit të ngadaltë të regjistrimit dhe pamundësisë për të prodhuar të dhëna të rëndësishme pas hedhjes në treg,” thanë kompanitë.
Aksionet e Pfizer dhe rivalit Moderna u rritën me rreth 1%, ndërsa aksionet e BioNTech të listuara në SHBA u rritën rreth 2%.
Shefi i vaksinave në FDA, Vinay Prasad, i cili kishte kërkuar prova të kontrolluara me placebo për të rritur të shëndetshëm dhe fëmijë, do të largohet nga agjencia këtë muaj. Ekspertët paralajmëruan se kërkesa për studime të reja të mëdha mund të vonojë ose kufizojë disponueshmërinë e vaksinave të përditësuara për grupet me rrezik më të ulët.
Nuk është e qartë se cila do të jetë rruga drejt miratimit për këtë grupmoshë. FDA nuk ishte menjëherë e disponueshme për koment. Kompanitë nuk komentuan mbi planet për tregtimin e vaksinës për këtë kategori.
Ndërprerja e studimit nga Pfizer dhe BioNTech vjen përpara një takimi të pritur në maj të komitetit këshillimor të FDA-së për vaksinat, i cili përdor të dhënat e studimeve për të orientuar vendimet mbi përzgjedhjen e varianteve të virusit për vaksinat e vjeshtës.
“Pa këto të dhëna, ndoshta nuk do të ketë prezantim,” tha Dr. Jesse Goodman, ish-shkencëtar kryesor i FDA-së. “Dhe pa prezantim, mund të mos ketë një miratim specifik për këtë grupmoshë.”
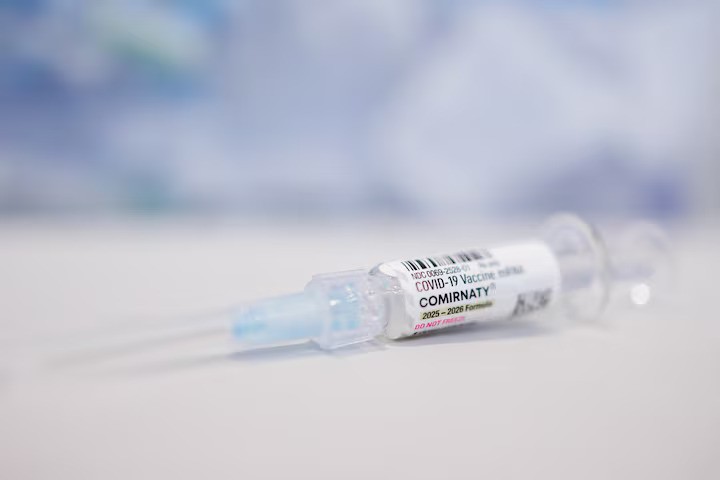
Një grup i vështirë për t’u rekrutuar
Dy burime nga kompani që menaxhojnë 18 nga 208 vendet e studimit thanë se Pfizer u kishte kërkuar me shkrim në fillim të marsit të ndalonin rekrutimin.
Studimi synonte të testonte efektivitetin, reagimin imunitar dhe sigurinë e vaksinës së përditësuar kundër COVID nga Pfizer dhe BioNTech tek të rritur të shëndetshëm 50–64 vjeç. FDA kërkonte që pjesëmarrësit të mos kishin sëmundje kronike si hipertension apo diabet.
“Ky është një grup shumë i vështirë për t’u rekrutuar,” tha një drejtues në një organizatë kërkimore me kontratë që ishte përfshirë në studim, duke folur në kushte anonimiteti.
“Edhe kur pacientët janë të gatshëm të marrin pjesë në studime për COVID, më shumë se 80% nuk kalojnë fazën paraprake sepse nuk plotësojnë kriteret shëndetësore. Ka qenë shumë e vështirë të regjistrohen mjaft pacientë, veçanërisht duke pasur parasysh përmasën e studimit,” tha ai.
Studimi i Moderna vazhdon; kërkesa për vaksina bie
Aktualisht, asnjë vaksinë kundër COVID nuk ka miratim të plotë nga FDA për të rritur të shëndetshëm 50–64 vjeç. Vaksinat Comirnaty dhe Spikevax, si dhe vaksina e gjeneratës së re mNEXSPIKE, janë të miratuara për të rritur mbi 65 vjeç dhe për persona më të rinj me rrezik të lartë për forma të rënda të sëmundjes.
Moderna po zhvillon një studim të ngjashëm në SHBA me synim regjistrimin e 30,000 vullnetarëve, por edhe ai po përballet me vështirësi në rekrutimin e pjesëmarrësve, sipas burimeve nga katër qendra studimi. Studimi pritet të përfundojë në qershor 2027. Moderna nuk iu përgjigj menjëherë kërkesës për koment.
Vaksinat kundër COVID mbeten produkte të rëndësishme për prodhuesit, megjithëse kërkesa ka rënë ndjeshëm që nga kulmi i pandemisë.
Vetëm rreth 18% e amerikanëve morën një dozë përforcuese gjatë sezonit 2025–26, sipas të dhënave nga CDC, edhe pse virusi vazhdon të shkaktojë dhjetëra mijëra vdekje çdo vit, përfshirë rreth 8,000 deri 12,000 vdekje tek të rriturit 50–64 vjeç.
Vaksinat e përditësuara kundër COVID për grupet e miratuara zakonisht autorizohen bazuar në të dhëna mbi reagimin imunitar, që tregojnë se sa mirë formula e re prodhon antitrupa kundër varianteve në qarkullim, një qasje e ngjashme me atë që përdoret për vaksinat sezonale të gripit, shkruan Reuters.